Nyt studie kaster lys over hvorfor nogle hjerneområder nedbrydes før andre i HS
Hvorfor dør kun visse hjerneceller i HS? Ny forskning viser, at det kan skyldes ineffektivt cellulært "genbrug"
Skrevet af Dr Kurt Jensen 22. november 2013 Redigeret af Dr Jeff Carroll Oversat af Signe Marie Borch Nielsen Oprindelig offentliggjort 12. november 2013
Nogle dele af hjernen degenererer hurtigere end andre hos personer med Huntingtons Sygdom. Steven Finkbeiners gruppe konkluderer, at dette skyldes, at der er forskel på hvor hurtige hjernecellerne i de forskellige hjerneområder er til at identificere og bortskaffe mutant HS-protein. Hjerneceller i de særligt udsatte områder i hjernen er længst tid om at skaffe sig af med proteinet.
Styr på foldningen
Proteiner er store biologiske molekyler, der udfører forskellige vigtige opgaver i cellen. Når et protein er blevet fremstillet ved at aminosyrer er blevet sat sammen i en bestemt rækkefølge i en lang kæde, bliver kæden foldet sammen som en kringle til en unik tredimensionel figur. Det er kun, når proteinet er foldet korrekt, at det kan udføre sine almindelige opgaver.
Desværre bliver nogle proteiner ændret, så de ikke længere bliver foldet korrekt. Ved HS sker der det, at en genetisk ændring (mutation) er skyld i, at en af aminosyrerne i huntingtin-proteinet (HTT), gentages igen og igen - lidt ligesom en plade der kører i hak.
Denne forlængede række af ens aminosyrer medfører, at HTT-proteinet bliver foldet forkert og dermed bliver giftigt for cellen og klumper sig sammen i store bunker, som forskerne kalder aggregater. Det er lidt ligesom en hårbolle, der tilstopper et afløb: løse, enkelte hår er ikke noget problem, men de store klumper stopper det til.
Hos patienter med HS indeholder alle celler i kroppen tilsyneladende mutant HS-protein, men det er hjernecellerne, der fortrinsvis dør ved sygdommen. Dette er grunden til, at HS kaldes en “neurodegenerativ” lidelse. Men faktisk dør alle hjerneceller heller ikke samtidig - det er primært specifikke typer hjerneceller i specifikke dele af hjernen, der dør til en start, hvilket tyder på, at de er de mest sårbare.
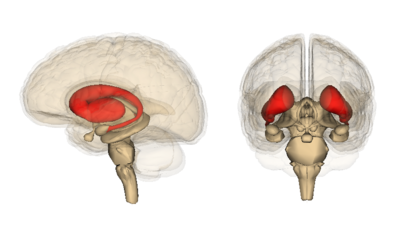
Den del af hjernen, hvor der tidligst og i højest grad sker celledød, kaldes striatum. Striatum findes dybt inde i midten af hjernen. Dens opgave er at koordinere bevægelser, tanker og sociale interaktioner, og at sikre, at der er styr på det hele.
Striatum er involveret i alt fra at stoppe en samtale til at stoppe en bevægelse. En ting som er ekstremt vigtig, men som man i øjeblikket ikke forstår er hvorfor dette hjerneområde så tidligt degenererer i HS, mens andre hjerneområder synes at håndtere det mutante HTT meget længere, før de bliver påvirket.
»Neuroner, der overfyldes med ekstra Nrf2 fjerner mutant HTT hurtigere end normalt og er mindre tilbøjelige til at dø. Dette tyder på, at det kunne være terapeutisk gavnligt ved HS at skrue op for cellens eget genbrugssystem. «
At smide skraldet og mutant huntingtin ud
To mulige forklaringer på disse forskelle blev undersøgt af et forskerhold ledet af Dr. Steven Finkbeiner ved University of California i San Francisco. En mulighed er, at der kan være forskel på, hvor hurtigt mutant HTT danner giftige strukturer i de forskellige celletyper i hjernen. Dybest set er det et spørgsmål om, hvor hurtigt løst hår bliver til hårboller i de enkelte celler.
En anden potentiel forklaring på det selektive tab af celler er, at de enkelte dele af hjernen måske har forskellig evne til at fjerne mutant HTT. Har nogle celler i virkeligheden bare rengøringsvanvid?
Forskerne opfandt en teknik, der gjorde dem i stand til at måle, hvor god hver enkelt hjernecelle var til at folde og fjerne protein. De fyldte cellerne med et lysende protein kaldet “Dendra2”. Dette protein er smart, fordi det normalt lyser grønt, men begynder at lyse rødt når det bliver belyst med en bestemt farve lys.
Så denne teknik gør det muligt at dyrke nogle neuroner i laboratoriet, som er fulde af grønt Dendra2-protein, og derefter “zappe” dem med lys, der får Dendra2-proteinerne til at lyse rødt. Man ser så på hvor lang tid det tager cellen at lave nyt, grønt Dendra2-protein og slippe af med det gamle, røde Dendra2-protein. Det siger noget om hvor hurtig cellen er til at lave nye proteiner (grønne), og nedbryde gamle (røde).
Selvfølgelig er det ikke Dendra2 vi rent faktisk bekymrer os om. Hvad vi i virkeligheden gerne vil vide, er, hvordan hjerneceller håndterer det normale HS-protein, og om dette ændres af mutationen, der forårsager HS. For at besvare dette spørgsmål, brugte forskerne nogle smarte laboratorietricks til at smelte enten et normalt eller mutant HS-protein sammen med Dendra2-proteinet. Dermed kunne de bruge det samme lys-trick til at følge HS-proteinet inde i cellen.
Skraldemanden klarer ærterne
Ved hjælp af dette system kunne forskerne se, at mutant HS-protein blev fjernet fra neuronerne i striatum meget hurtigere end det normale Htt. Dette er overraskende - mange forskere ville have troet, at den mutante form af proteinet blev i cellen længere, og at det var dette, der fik proteinet til at ophobes i aggregater. Disse resultater tyder snarere på, at neuronerne er i stand til at genkende det mutante protein og gå målrettet efter at fjerne det.
Faktisk kunne Finkbeiners forskerhold ved hjælp af et specialudviklet mikroskop se, at jo hurtigere en celle fjernede det mutante Htt-protein, jo længere levede den. Det giver mening - at skaffe sig af med det giftige skrald beskytter hjernecellerne.
Så hvis cellen rent faktisk er i stand til at genkende og indsamle mutant protein, hvad er problemet så? Det viser sig, at nogle neuroner er bedre til at rydde op end andre, nemlig dem der findes i cortex. Cortex (eller hjernebarken) er hjernens rynkede yderside. Generelt bukker cellerne i cortex under for HS senere end cellerne i striatum. I håbet om at forstå hvorfor, sammenlignede forskerne hvordan mutant HS-protein blev fjernet i henholdsvis striatum og cortex.
»Det vigtigste ved dette studie er, at neuroner fra forskellige hjerneområder ikke er lige gode til at håndtere mutant Htt. Dette kan være en forklaring på hvorfor HS starter i nogle hjerneområder og ikke i andre. «
Det viste sig, at neuronerne i cortex kunne slippe af med mutant HTT hurtigere. Neuronerne i cortex levede også længere end neuronerne i striatum. Forskerholdet konkluderede, at dette skyldes, at der er forskel på hvor gode de forskellige hjernedele er til at rydde ud i det mutante HS-protein.
Når proteiner bliver gamle eller slidte, har cellen et system til at fjerne eller genbruge dem. Forskerne undersøgte, om deres observationer kunne skyldes, at dette nedbrydningssystem er påvirket. De fokuserede især på Nrf2, et protein, der aktiverer genbrugsprocessen.
Forskere kan studere, hvordan forskellige cellulære processer bidrager til celledød og genanvendelse af proteiner ved at skrue op for aktiviteten af en bestemt proces eller hæmme den. I dette tilfælde valgte de enten at give mere Nrf2 eller at fjerne det helt, fordi de mente, at de genbrugsprocesser Nrf2 styrer, er vigtige. Det hjalp dem altså til at se, om en bestemt proces var vigtig eller ej.
Det viste sig, at neuroner som fik ekstra Nrf2 fjernede mutant Htt-protein hurtigere end normalt, og var mindre tilbøjelige til at dø. Dette tyder på, at det at skrue op for cellens egne genbrugsprocesser kunne være et potentielt mål for behandling i HS.
I overensstemmelse med denne idé sås det, at cellerne blev dårligere til at fjerne mutant HS-protein når forskerne kunstigt reducerede cellens primære skralde- eller genbrugssystem med forskellige kemiske stoffer. Så denne specifikke genbrugsproces synes at være afgørende for, at neuroner kan håndtere det giftige protein ordentligt.

Hvad betyder dette for HS?
Det vigtigste, der blev fundet ved denne undersøgelse var, at neuroner fra forskellige områder af hjernen ikke er lige gode til at håndtere mutant HTT. Det kan være en forklaring på, hvorfor HS begynder i ét område af hjernen og ikke i et andet. Det gode ved denne opdagelse er, at denne følsomhed synes at være baseret på forskelle i neuronernes evner til at håndtere og skille sig af med det mutante protein, snarere end en iboende toksicitet af proteinet selv.
Det er faktisk meget vigtigt, fordi det giver interessante muligheder for at udvikle lægemidler, der påvirker neuronernes evne til at hådtere mutant HTT. Ud fra resultaterne af denne undersøgelse, vil vi gætte på, at behandlinger, der forbedrer neuroners evne til at fjerne mutant HTT vil få dem til at leve længere.
Men denne interessante mulighed skal selvfølgelig ses i det rette lys. For det første blev hele dette studie udført ved hjælp af neuroner, der blev dyrket i en skål. Det er stadig uvist, om dette fænomen også gør sig gældende ved HS i mennesker, som er det, der betyder mest.
For det andet er disse resultater indledende - de potentielle behandlinger beskrevet ovenfor eksisterer endnu ikke. Det vil tage tid at udtænke en passende behandling og teste den i andre HS-modeller, før den kunne afprøves i mennesker. For eksempel ved ingen, hvilke skadelige bivirkninger der kan opstå, hvis Nrf2-systemet blev kunstigt stimuleret over lang tid.
Summa summarum: disse observationer er grundlæggende meget spændende HS-videnskab. Og da der stadig ingen godkendte lægemidler findes, som kan behandle det grundlæggende problem i HS, så giver undersøgelser som denne en bedre forståelse for denne frygtelige sygdom, hvilket forhåbentlig kan bane vejen for udviklingen af nye lægemidler.