En magtfuld budbringer: forårsager et giftigt RNA budbringermolekyle skade ved Huntingtons Sygdom?
Hvad nu hvis nogle problemer ved HS skyldes noget andet end et skadeligt protein?
 Skrevet af Dr Jeff Carroll 23. maj 2017 Redigeret af Professor Ed Wild Oversat af Mette Gilling Nielsen Oprindelig offentliggjort 23. december 2016
Skrevet af Dr Jeff Carroll 23. maj 2017 Redigeret af Professor Ed Wild Oversat af Mette Gilling Nielsen Oprindelig offentliggjort 23. december 2016
Forskere har længe antaget, at HS-genet forårsager problemer, fordi det får cellerne til at danne et skadeligt protein. Interessante nye dyreforsøg, udført af forskere i Spanien, tyder på, at vi nok bør kigge på mere end én mistænkt for helt at løse de problemer, som HS-mutationen forårsager.
Det centrale biologiske dogme
Alle patienter med Huntingtons Sygdom bærer grundlæggende den samme genetiske ændring (mutation) arvet fra enten deres mor eller far. Denne mutation er i et gen, vi for det meste bare kalder HS-genet, for at holde det enkelt.
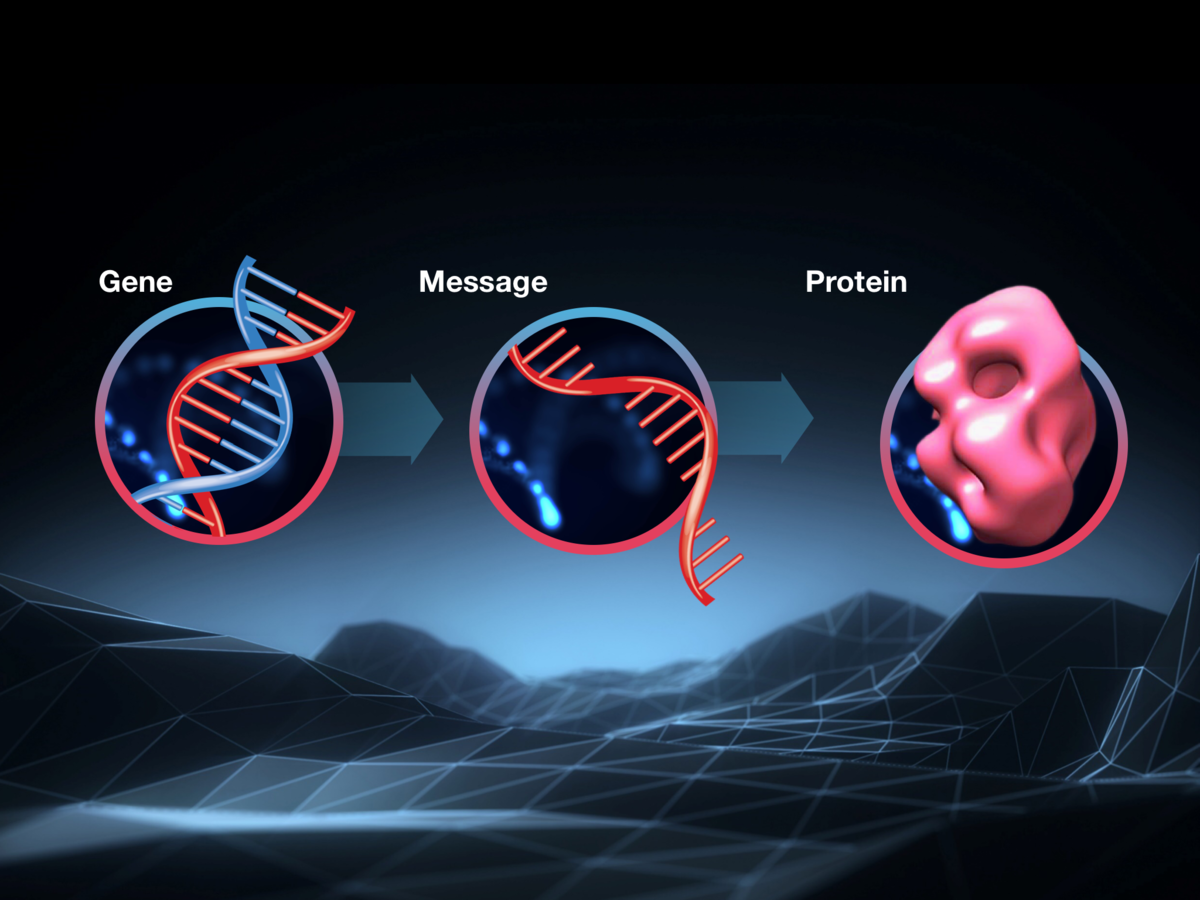
Den mutation, der forårsager HS, er en forlængelse af en DNA-sekvens, der allerede er gentaget i HS-genet. Nær den ene ende af genet finder vi de genetiske bogstaver C-A-G gentaget igen og igen. Hos mennesker uden Huntingtons Sygdom indeholder deres HS-gener ca. 20 gentagelser af denne CAG-sekvens. Men hvis du arver en kopi af HS-genet med mere end 39 gentagelser, vil du udvikle Huntingtons Sygdom på et eller andet tidspunkt i dit liv.
Celler bruger gener som instruktioner eller opskrifter til at lave proteiner. Proteiner er de maskiner, der får cellerne til at fungere. Alle de seje ting vores celler kan, afhænger af de indviklede interaktioner mellem de tusindvis af forskellige proteiner, der hvirvler og suser omkring inde i hver eneste celle.
For at komme fra instruktionerne i vores gener til proteinerne, der laver alt muligt inde i cellerne, skal man igennem et ekstra trin. Fordi DNAet er så vigtigt og skal beskyttes for enhver pris, kopierer cellen instruktionen over i et molekyle kaldet RNA, som bruges til at lave det protein, der er brug for.
Da disse RNA-molekyler bærer information fra ét sted i cellen til et andet, kalder forskere disse ‘messenger RNA’ eller mRNA.
Når mRNA flyder rundt, bliver det læst i cellen og instrukserne bliver fulgt for at lave det tilsvarende protein. Denne arbejdsgang fra gen over mRNA til protein er den måde proteiner bliver dannet og kontrolleret på i alle celler. Det er så grundlæggende, at det nogle gange kaldes 'det centrale biologiske dogme’.
Hvem er skurken?
Hvilke af disse spillere er skurken? De fleste forskere, der arbejder med HS, mener, at det er det mutante protein og ikke genet eller mRNAet, der forårsager de fleste af de problemer, der ses i cellerne hos mennesker, der bærer mutationen for Huntingtons Sygdom. Og der er tonsvis af beviser på, at proteinet er skyld i mange af de ting, der går galt i celler, der bærer HS-mutationen. Men er det hele sandheden?
I nogle andre genetiske sygdomme er det mRNAet selv, der er hovedårsagen til problemerne. Et eksempel er sygdommen muskeldystrofi (muskelsvind), der også skyldes for mange gentagelser af en genetisk sekvens med tre bogstaver. Ved muskeldystrofi får mRNAer med mange gentagelser cellerne til at fungere dårligt og i sidste ende dø - her er det mRNAet, der bærer skylden, ikke det tilsvarende protein.
Der har længe været en gruppe forskere, der har troet på, at mRNAet også kunne være skadeligt i Huntingtons Sygdom. Nye undersøgelser fra en forskergruppe i Spanien tyder på, at disse tænk-ud-af-boksen-forskere kan have ret.
Det første arbejde i celler
I 2012 beskrev en gruppe forskere, under ledelse af Eulalia Marti fra ‘University of Barcelona’, nogle meget interessante undersøgelser, de havde lavet med HS mRNAet. De opdagede, at mRNA-molekyler lavet fra mutante HS-gener - de mRNAer, der findes hos mennesker, der udvikler Huntingtons Sygdom - kunne være giftige for celler i laboratoriet. mRNA-molekyler fra normale gener var ikke giftige for celler.
Det var overraskende, fordi gruppen havde sørget for, at de mRNA-molekyler, de undersøgte, ikke kunne instruere cellen i at lave mutant protein. Gruppen lavede også nogle detaljerede opfølgende forsøg og identificeret nogle af de centrale aktører i cellen, der er årsag til, at mRNAet er giftigt.
Men bare fordi noget kan ske i celler i en petriskål, betyder det ikke, at det sker i levende hjerner, så Martis hold rettede derfor deres opmærksomhed på en musemodel af Huntingtons Sygdom og hjerner fra rigtige HS-patienter. I syge områder af hjernen hos både mus og mennesker, fandt de tegn på giftige stykker af HS mRNA-molekylet. Da de omhyggeligt fjernede alle proteiner og andre ting fra disse rigtige hjerner, så kun mRNA-molekylerne var tilbage, fandt de ud af, at disse mRNA-molekyler kunne få sunde celler i laboratoriet til at blive syge.
Dette er et ret godt bevis på, at noget interessant sker med HS mRNA-molekylet, og at det er meget muligt, at nogle af årsagerne til, at cellerne bliver syge i HS, kan skyldes andet end det mutante protein.
»Dette nye studie benytter en smart metode til at vise, at budbringeren måske kan være skadelig, og at den forvoldte skade muligvis betyder noget. «
Nye undersøgelser i mus
For nyligt har Martis hold offentliggjort en meget interessant opfølgningsundersøgelse, der tyder på, at de kan være på sporet af noget vigtigt. Den nye undersøgelse benytter en smart metode til at vise, at mRNAet kan være skadeligt, og at den skade kan være af betydning.
Marti og hendes gruppe fandt på en måde at forhindre HS mRNAet i at være giftigt uden at ændre mængderne af det protein, der bliver dannet fra HS-genet. Med andre ord er mRNAet der stadigvæk og kan læses af det maskineri i cellerne, der fremstiller proteiner, men det kan ikke direkte forårsage skade.
Overraskende nok fandt de en måde at gøre dette på ved at bruge noget, der hedder et antisense oligonukleotid eller ASO.
Hvis du allerede har hørt om ASO'er, er det sandsynligvis fordi de i øjeblikket afprøves i mennesker med Huntingtons Sygdom som en potentiel behandling. Generelt er opgaven for ASO'er at finde vej ind i cellerne og klistre sig til mRNA-molekyler.
De ASO'er, der i øjeblikket afprøves i mennesker, er fremstillet af Ionis Pharmaceuticals og binder sig til mRNAet fra HS-genet, hvorved det bliver sendt til destruktion. Færre mRNA-molekyler betyder færre proteiner - og vi håber, at det vil beskytte cellerne mod skade. Denne tilgang kaldes huntingtin nedregulering eller undertiden genhæmning.
De ASO'er, Marti og hendes kolleger benyttede, fungerer marginalt anderledes. De bevæger sig ind i cellerne og finder HS mRNA-molekylerne, men når de finder dem, klistrer de bare fast til dem og hænger ud. Ingen HS mRNA-molekyler bliver ødelagt, så der er ingen ændring i mængderne af proteinet.
Hvad skal man dog med sådan en ubrugelig ASO? Martis gruppe fandt ud af, at ved at binde en ASO til HS mRNAet, blev mRNAets giftige virkninger, som de havde kortlagt i deres tidligere undersøgelse, blokeret. De fandt altså et rigtig godt værktøj til at undersøge, hvilken rolle mRNAet spiller i sygdomsudviklingen.
Da de sprøjtede denne særlige ASO ind i hjernerne på HS-mus, blev de giftige effekter af mRNAet reduceret, men der var ingen ændring i niveauet af HS-proteinet, som de havde forudsagt. Overraskende nok fandt de ud af, at musene virkede til at have det meget bedre, selvom der stadig var masser af mutant HS-protein.
Hvad betyder alt det her?
Dette er virkelig sej videnskab, fordi det er gjort meget omhyggeligt og husker os på, at vi skal blive ved med at stille spørgsmålstegn ved vores antagelser om, hvordan HS fungerer. Ethvert problem, der er så komplekst som HS, vil sandsynligvis have flere årsager - og det er meget sandsynligt, at både mRNAet og proteinet skabt fra det mutante HS-gen kan være giftigt.
Hvad betyder dette for HS-behandlinger, især det igangværende huntingtinsænkende forsøg med ASO'er? Vi ved det ikke endnu, men intuitivt giver det mening, at en ASO af den type, der testes af Ionis, skulle hjælpe på begge typer giftige effekter - både dem, der er forårsaget af mRNAet og dem, der er forårsaget af proteinet. Man ville tilsvarende forvente, at mange andre tilgange til at sænke huntingtinmængden også ville slippe af med både det giftige mRNA og protein. Og selvom nogle fremtidige behandlinger “kun” reducerer proteinniveauet, er vi stadig temmelig sikre på, at det ville være en rigtig god ting at gøre. Sikke en lettelse!
Nu hvor Marti og hendes gruppe har vist vejen, kan forskere i fremtiden undersøge, hvordan nye potentielle behandlinger påvirker begge mulige former for toksicitet forårsaget af HS-mutationen.