Genhæmningslægemiddel er sikkert i ALS-patienter....sæt gang i afprøvninger i patienter med Huntingtons Sygdom
Genhæmningslægemiddel injiceret i spinalvæsken på ALS-patienter viser sig at være sikkert. God nyhed før HS-forsøg.
Skrevet af Joseph Ochaba 15. november 2013 Redigeret af Professor Ed Wild Oversat af Mette Gilling Nielsen Oprindelig offentliggjort 29. juni 2013
Genhæmmende lægemidler, der giver cellerne ordre til at stoppe med at lave det skadelige huntingtin-protein, er en af de tilgange til at bekæmpe Huntingtons Sygdom, der arbejdes mest på. Et klinisk studie med et ‘ASO’ genhæmmende lægemiddel i mennesker med motorneuron sygdom har netop vist, at leveringsmetoden og lægemidlet er sikkert, hvilket har sat gang i planerne om at få kliniske forsøg med disse lægemidler op at køre i HS.
Gen-tavshed er guld
Unormale eller mutante proteiner forårsager mange hjernesygdomme, herunder Huntingtons Sygdom (HS). ‘Genhæmmende’ lægemidler er designerlægemidler, der giver cellerne ordre til at stoppe med at lave et særligt skadeligt protein. Et gen er en opskrift på ét protein, men cellerne laver en ‘arbejdskopi’ af genet, der indeholder instruktioner, der bliver læst igen og igen for at bygge det givne protein mange gange. Genhæmningslægemidler er omhyggeligt designet til at hæfte sig til arbejdskopien for et udvalgt protein, så det ikke kan læses og derfor medfører, at mindre af dets protein bliver lavet.

Genhæmningslægemidler er i øjeblikket formentlig den mest lovende tilgang til at bekæmpe Huntingtons Sygdom. Mange genhæmningslægemidler har fungeret godt i dyremodeller for HS. Der er flere ‘varianter’ af genhæmning, der bruger lidt forskellige kemiske strukturer og metoder til at få lægemidlet ind i hjernen.
Denne artikel handler om et patientforsøg med antisense-oligonukleotider eller ASOer. ASOer er en bestemt form for genhæmning, der er i stand til at sprede sig ganske godt gennem nervesystemet, når de injiceres i cerebrospinalvæsken (væske, der omgiver hjernen og også løber ned i rygraden), og er i stand til at krydse vores hjernes ‘grænseovergang’ kendt som blod-hjerne-barrieren - der oftest udgør et stort problem for forskerne når de udvikler lægemidler imod hjernesygdomme.
Hvem er Lou?
Patienterne i denne kliniske afprøvning havde en sygdom, der går under tre navne - amyotrofisk lateral sklerose (ALS), motorneuronsygdom og Lou Gehrig sygdom. Gehrig var en berømt baseballspiller, der led af denne sygdom, der påvirker nerveceller i hjernen og rygmarven og i sidste ende fører til lammelse og død.
Ved Huntingtons Sygdom har alle patienter den samme genetiske ændring i det gen, der producerer huntingtinprotein. I ALS har kun en lille procentdel af patienterne en kendt genetisk mutation. Omkring 2% har en særlig mutation i et protein kaldet superoxiddismutase 1 (SOD1), som forårsager en familiær eller arvelig form af sygdommen.
Mens der arbejdes på at udvikle ASO genhæmnings-lægemidler til Huntingtons Sygdom, er det første forsøg med ASOer i mennesker til behandling af en sygdom i nervesystem lige blevet afsluttet for ALS. Forsøget var et samarbejde mellem forskere fra ‘Washington University School of Medicine’, ‘Massachusetts General Hospital’, ‘Johns Hopkins University’ og ‘Methodist Neurological Institute’ i samarbejde med ‘Isis Pharmaceuticals’. Resultaterne blev for nylig rapporteret i tidsskriftet Lancet Neurology.
Forskerne satte sig for at teste sikkerhedsprofilen for eksperimentelle ASOer, der har til formål at lukke SOD1-genet ned. Alle patienter var blevet genetisk testet og havde mutationer i SOD1, der forårsagede deres ALS. For første gang blev ASOer sprøjtet direkte ind i cerebrospinalvæsken (CSF), der omgiver hjernen og rygmarven.
Hvordan gjorde de det?
»ASOer udgør en særlig variant af genhæmning, der ser ud til at sprede sig ganske godt igennem nervesystemet når de injiceres i cerebrospinalvæsken «
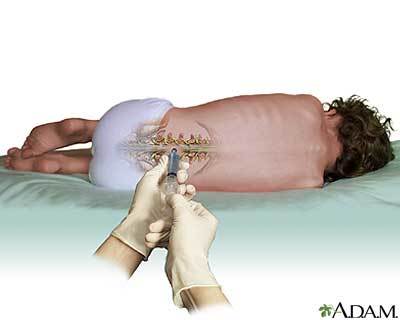
20 ALS-patienter blev inddelt i 4 forskellige grupper i denne kliniske afprøvning. I hver gruppe fik nogen patienter et inaktivt ‘placebo’-lægemiddel mens andre fik det aktive lægemiddel. Dosis af lægemidlet var forskellig i hver gruppe. En lille elektronisk pumpe blev indopereret under huden, så den langsomt, men kontinuerligt, kunne levere små doser af lægemidlet igennem et kateter til cerebrospinalvæsken. Dette er meget lig det, man gør, når kvinder får en epiduralblokade under en fødsel, men det varede bare i meget længere tid.
Sikkerheden først!
En vigtig ting at bide mærke i er, at målet for dette kliniske studie ikke var at se, om dette ASO-lægemiddel kunne kurere ALS eller ej, men derimod at undersøge sikkerheden, og hvor godt en enkelt dosis af det ASO-lægemiddel, der kan nedregulere SOD1, kunne tolereres. Ydermere ville forskerne undersøge om pumpesystemet gjorde, at lægemidlet krydsede blod-hjerne-barrieren mere effektivt. Efter den kliniske afprøvning konkluderede forskerne, at sikkerhedsprofilen så vældig god ud. Ingen deltagere i studiet havde alvorlige problemer af hverken sikkerheds- eller tolerancemæssig karakter i forbindelse med proceduren eller indsprøjtningen af test-ASOer. En af de mest almindeligt rapporterede bivirkninger var en eller anden form for ondt i hovedet eller ondt i ryggen efter selve proceduren med indsprøjtning af lægemiddel og aftapning af CSF-væske, men dette havde sandsynligvis ikke noget med selve lægemidlet at gøre. Ud over at kigge på lægemidlets sikkerhedsprofil efter injektion, så tog forskerne også prøver for at tjekke, at nedreguleringslægemidlet blev fordelt rundt i patienternes cerebrospinalvæske, og at mængden af lægemidlet øgedes efter behandling for derefter hurtigt at blive fjernet af kroppen - hvilket alt sammen var tilfældet.
Ramte de målet?
Da formålet med ASO-lægemidlet er at nedsætte mængden af SOD1-protein, er det vel rimeligt at spørge, om det så virkede eller ej. Men husk på, at dette var et sikkerhedsstudie, hvis formål var at finde ud af, om det er farligt at sprøjte ASOer ind i nervesystemet. Forskerne havde ikke rigtig nogen forventning om, at deres lægemiddel, der kun blev givet i lave doser og i korte perioder, ville ændre mængden af det mutante SOD1-protein. De undersøgte mængden af SOD1-protein i CSF, men fandt ingen ændringer. Alle doser af lægemidlet var lave og højere doser vil sandsynligvis være nødvendige i fremtidige studier for effektivt at ‘lukke ned’ for det giftige protein.
Flere spor
Forskerne kunne undersøge SOD1-mængden i rygmarven fra én af deltagerne i studiet, idet vedkommende døde af ALS få måneder efter behandlingen. Forskerne fandt ud af, at når de sammenlignede niveauet af SOD1-protein i vævet fra denne patient med niveauet hos andre ALS-patienter, så lå det i den lave ende af normalområdet. Ydermere kunne ASO-lægemiddel stadigvæk detekteres i personens rygmarv, hvilket tyder på, at ASO-lægemidler kan forblive i vævet i ret lang tid.
Hvad bliver det næste?
ASO-lægemidlet i dette studie var udviklet og produceret af ‘Isis Pharmaceuticals’. En del af deres succes kan tilskrives de kloge kemiske ændringer, de har lavet til deres ASOer, idet det får dem til at holde længere i kroppen og binde bedre til deres mål. Firmaet arbejder på at lave ASOer til at behandle forskellige sygdomme, inklusiv Huntingtons Sygdom. I forbindelse med SOD1-nedregulering i ALS, planlægger de kemisk at finjustere ASOerne inden yderligere sikkerheds- og lægemiddelstudier påbegyndes, sandsynligvis med højere doser og længere behandlingstider.
Når dosis øges, vil der blive holdt øje med at behandlingen ikke forårsager skader på hjernen eller andre bivirkninger, samtidig med at det sænker SOD1-proteinniveauet.
Hvad med Huntingtons Sygdom?
Enhver god nyhed om genhæmning ventes med spænding af medlemmer af familier med Huntingtons Sygdom. Men det er værd at huske os selv på, at det stof, der blev brugt i dette forsøg, ikke ville fungere ved HS, fordi det rammer SOD1-proteinet og ikke det mutante huntingtin-protein. Lægemidler til Huntingtons Sygdom skal udvikles særskilt og gennemgå deres egne sikkerhedstests.
Det er også vigtigt at bemærke, at det lille antal deltagere i denne undersøgelse begrænser hvilke konklusioner, der kan drages om sikkerheden, selv for brugen af dette specifikke ASO-lægemiddel i ALS. Sjældne bivirkninger vil muligvis ikke forekomme i sådan en lille gruppe.
Som vi rapporterede i april, har ‘Isis Pharmaceuticals’ for nyligt lavet en kæmpe millionaftale ($30) med medicinalfirmaet Roche om at samarbejde om at få deres huntingtin nedregulerende ASOer i kliniske forsøg for Huntingtons Sygdom. Isis har udført et vellykket sikkerhedsstudie af et huntingtin-dæmpende ASO-lægemiddel i primater - et stort skridt på vejen til at få et lægemiddel godkendt til forsøg i mennesker. I øjeblikket finpudser Isis stadig sine lægemidler til HS og skal beslutte hvilket, der er bedst at arbejde videre med i mennesker.
Så de opmuntrende resultater fra dette studie i ALS-patienter giver værdifuld indsigt, som vil være en hjælp i planlægningen af de huntingtin ASO genhæmningsforsøg for patienter med Huntingtons Sygdom, der er planer om at udføre i den nærmeste fremtid.