Nye resultater bringer BDNF-behandlinger i fokus
Nye, uventede resultater foreslår nye måder at ramme et gammelt mål på ved HS
 Skrevet af Dr Jeff Carroll 26. september 2014 Redigeret af Dr Tamara Maiuri Oversat af Rasmus Siersbæk Oprindelig offentliggjort 18. august 2014
Skrevet af Dr Jeff Carroll 26. september 2014 Redigeret af Dr Tamara Maiuri Oversat af Rasmus Siersbæk Oprindelig offentliggjort 18. august 2014
Cellerne i hjernen har brug for støtte fra hinanden for at overleve. Næringsstoffer kaldet trofiske faktorer fungerer som gødning for hjernen, hvilket medvirker til, at hjernecellerne kan holde hinanden raske. Man har længe troet, at denne proces går galt i HS, og spændende ny museforskning maler et meget klart billede af præcis, hvad der sker.
Hjerneføde
Specifikke hjerneceller, kaldet neuroner, fungerer ved at sende beskeder til hinanden hvorefter de bruger disse beskeder til at lave beregninger. Enhver aktivitet i dyreriget, fra en orm, der kravler gennem mudderet til et menneske, der skriver et digt, afhænger af at disse celler taler med hinanden. Ved samlingerne mellem neuroner, kaldet synapser, strømmer kemiske beskeder hurtigt fra de celler, der sender til de celler, der modtager.
De kemiske beskeder, der sendes mellem neuroner bliver normalt kaldet neurotransmittere - de er ansvarlige for de millisekund-til-millisekund kommunikationer, der foregår i hjernen. Ud over denne “plapren” af neutroansmittere findes andre kemiske beskeder, der sendes af én celle og modtages af en anden. Helt på samme måde som når en ledning fra dit TV-selskab kan indeholde flere kanaler så foregår der også mere end én type kommunikation over synapserne mellem neuronerne.
En af disse alternative kanaler indeholder signaler, som forskere kalder neurotrofiske faktorer. Disse er store, komplekse kemikalier, der, i modsætning til neurotransmittere, som formidler normal kommunikation mellem hjerneceller, stort set kun siger én ting: “Hold dig i live!”
Dette virker en smule mærkeligt - hvorfor skulle hjerneceller nogensinde have lyst til at dø? I virkeligheden er en af de mærkeligste ting omkring menneskets hjerne, at omkring halvdelen af alle de celler, der nogensinde bliver dannet i din hjerne, dør før du bliver voksen. Dette virker som et spild, men det er en proces, der er blevet udviklet under evolutionen til at sørge for, at vores hjerner forbliver fyldte med raske, højt forbundne neuroner.
Selv i den voksne hjerne vil en celle, der er adskilt fra sine naboer simpelthen dø. En af de vigtigste måder vores hjerner kontrollerer denne proces på, er ved at programmere hjernecellerne til at blive ‘afhængige’ af de store kemikalier, der frigives ved synapser sammen med de normale neurotransmitettere. Da deres job er at holde neuroner raske, kalder forskere disse vigtige kemikalier neuro-trofiske faktorer (-trof er græsk for at ‘nære’ eller ‘fodre’).
Som et resultat af dette tilsyneladende mærkelige design er vores hjerner en konstant boblende gryderat af neurotrofiske faktorer, hvor hver neuron konstant råber til sine naboer, “Hey! Hold jer i live!”
Der findes et stort antal neurotrofiske faktorer med en forvirrende alfabetsuppe af akronymer til at identificere dem med (BDNF, GDNF, CNTF, TNF, TGF og så videre). En af disse faktorer, kaldet ‘brain-derived neuro-trophic factor’, eller BDNF, er specielt interessant i forhold til Huntingtons Sygdom.
Kritisk kredsløb i HS-hjernen
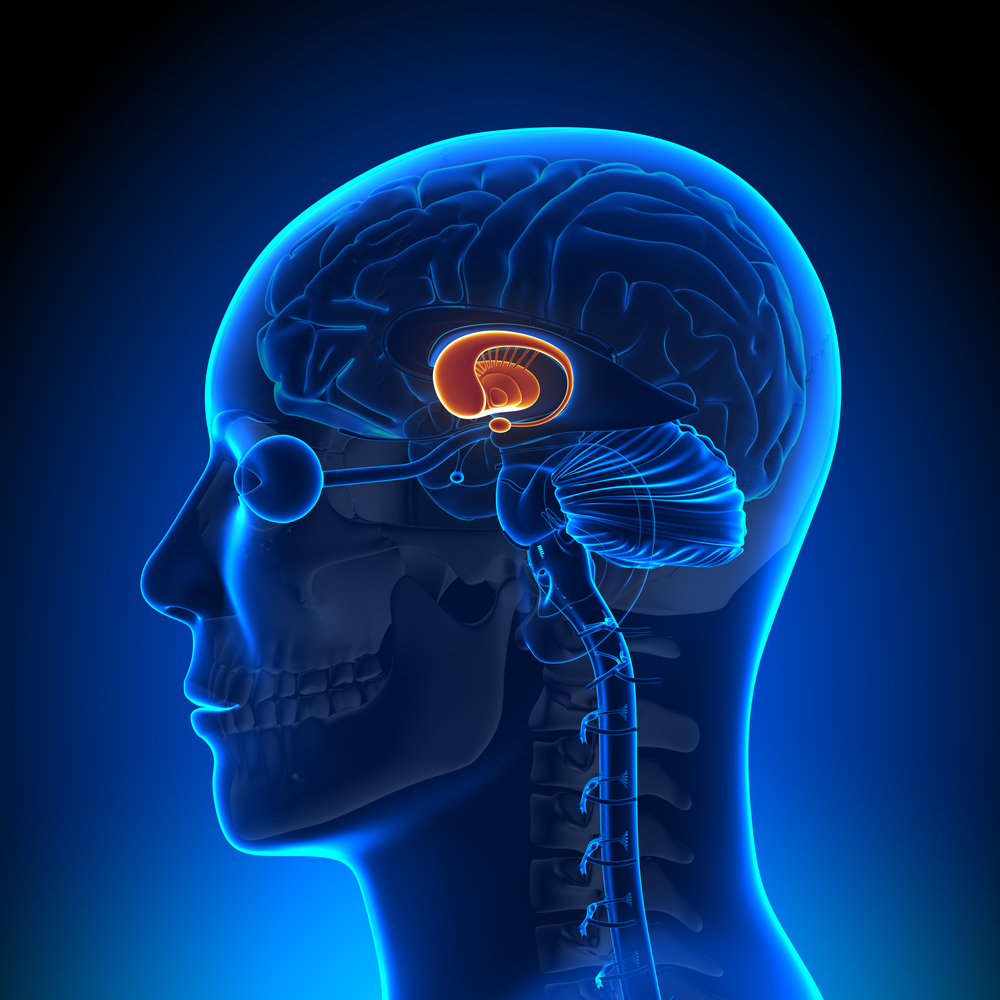
HS er associeret med meget specifikke mønstre af celledød i hjernen. Dybt under overfladen af hjernen findes en lille gruppe celler kaldet striatum, der ser ud til at være den mest sårbare region, som degenererer næsten fuldstændigt i løbet af livet hos en person med HS.
Ligesom de fleste andre regioner af hjernen, der er forbundet med hinanden i komplekse kredsløb, så modtager striatum input fra cortex - den karakteristiske, rynkede overflade, som er mest tydelig når man ser hjernen udefra. Forskere mener, at sammenbrud af kommunikationen mellem disse to dele af hjernen (cortex og striatum) måske kan forklare de fleste symptomer ved HS.
Som ved mange andre forbindelser i hjernen er kommunikationen mellem cortex og striatum associeret med frigivelse af en trofisk faktor - i dette tilfælde BDNF. Celler i cortex fodrer celler i striatum med BDNF, hvilket konstant minder dem om, at de ikke må dø.
Da hjerneceller i striatum ser ud til at være sårbare i HS-patienter, var det interessant for HS-forskere at undersøge denne neurotrofiske proces. Hvis levering af BDNF fra cortex til striatum på en eller anden måde var svækket i HS, kunne det så forklare sårbarheden af striatum?
Tidligere BDNF-undersøgelser
Allerede i 2001 fandt en gruppe HS-forskere (ledet af Professor Elena Cattaneo i Milano) faktisk ud af, at celler med det muterede HS-gen så ud til at producere mindre BDNF. Efterfølgende undersøgelser udført af et hold forskere ledet af Professorerne Sandrine Humbert og Frederic Saudou i Frankrig antydede, at celler med det muterede HS-gen også så ud til at have problemer med det maskineri, der står for at transportere BDNF ud af cellerne.
Efterfølgende har et stort antal studier antydet, at en forøgelse af mængden af BDNF i hjernen, gennem en forvirrende række af metoder, gør, at HS-mus får det bedre. Det er står derfor rimelig klart, at når det kommer til BDNF så er mere bedre for celler i HS-striatum.
Overraskende nye resultater
Et nyt studie af en gruppe forskere (ledet af Prof James Surmeier fra “Northwestern University i Chicago”) tilfører vigtige detaljer til BDNF-historien. Surmeiers hold brugte sofistikerede teknikker til at studere individuelle synapser mellem neuroner i musehjerner. Lasere monteret på deres komplekse mikroskoper gør dem i stand til at aktivere individuelle synapser og studere, hvordan disse synapser er forandrede ved HS.
»Overraskende nok fandt Surmeiers hold ikke nogen forskelle i den mængde BDNF, der bliver produceret i cortex eller i den mængde, der landede på neuroner i striatum «
I en normal hjerneproces som indlæring kunne Surmeiers hold observere forstærkningen og svækkelsen af individueller synapser - normale ændringer, der ligger til grund for læringsprocessen.
Denne fleksibilitet i den raske synapse fandtes ikke i specifikke synapser i HS-mus, hvilket indikerer dårlig kommunikation mellem cortex og striatum. Hvad er det, der gør, at synapser i HS-hjernen ikke udfører deres job ordentligt?
Surmeiers hold var opsatte på at finde ud af, hvad der kunne forårsage denne svage kommunikation mellem cortex og striatum. Motiverede af tidligere resultater undersøgte holdet frigivelsen af BDNF.
Overraskende nok fandt Surmeiers hold ikke nogen forskelle i den mængde BDNF, der blev produceret i cortex eller i den mængde, der landede på neuronerne i striatum i de HS musehjerner, de studerede. Dette var meget anderledes end hvad andre grupper havde observeret.
Det er ikke dig, det er mig
Betyder dette, at BDNF ikke betyder noget? Surmeiers hold dykkede en smule dybere og kiggede på de typer forandringer, der sker inde i modtagercellen, når BDNF lander på den.
For at kemikalier såsom neurotransmittere og trofiske faktorer kan have en effekt på modtagercellen, skal de genkendes på modtagerens side. Denne genkendelse opnås, når modtagercellen producerer en specifik receptor for hvert specifikke signal. Hvis BDNF i dette tilfælde er nøglen, er ‘BDNF receptorer’ de nøglehuller på celleoverfladen, hvori den passer.
Som om historien ikke allerede var kompliceret nok så viser det sig, at BDNF faktisk har tre (eller flere!) forskellige nøglehuller, den kan passe i på overfladen af modtagercellen. Naturen er forunderlig! Måske sender nogle BDNF-receptorer de kritiske ‘hold dig i live’-beskeder, mens andre fortæller cellen: “du kan dø nu!” med det ultimative mål at vedligeholde disse raske, højt forbundne neuroner.
Tak til naturen for at være så kompliceret.
Her er den let forståelige versionen af, hvad Surmeiers hold opdagede: Celler i cortex hos HS-mus lavede tilstrækkeligt BDNF. Celler i striatum hos HS-mus modtog fuldstændig lige så meget ‘hold dig i live’-signal som dem hos normale mus. Men HS-mus modtog også en ekstra dosis af den ‘dø nu’ besked som BDNF kan sende.
Når forskerne blokerede de BDNF-receptorer, der starter ‘dø nu’-beskeden, fandt de ud af, at cellerne i striatum i HS-mus blev mere fleksible og derved lignede dem i normale mus.
Er dette godt nyt aller dårligt nyt?
Rapporten fra Surmeier og hans hold ser måske ved første øjekast ud til at komplicere tingene. Da de startede med at studere BDNF, regnede de med at finde én specifik type dysfunktion, men de fandt faktisk noget helt andet.
Men dette er faktisk et stort fremskridt, fordi det hjælper os til i meget større detaljegrad at forstå hvad der sker med BDNF i disse HS-mus. Fremtidige studier vil klargøre, hvorfor forsøg med forskellige typer HS-mus har givet forskellige resultater, hvilket sandsynligvis vil hjælpe forskere til bedre at forstå rollen af BDNF i HS.
Mest spændende er det dog, at dette studie har givet et nyt mål for udvikling af lægemidler mod HS. I stedet for at prøve at øge mængden af BDNF i hjernen er forskere måske i stand til simpelthen af blokere den specifikke BDNF-receptor, der fortæller cellerne ‘dø nu’. Fordi BDNF-signalering gennem ‘hold dig i live’-kanalen stadig foregik, kan vi måske forvente, at denne form for behandling kunne gøre, at HS-mus fik det bedre. Hold øje med mere spændende arbejde om BDNF i fremtiden.